硫酸盐离子(SO42 -)是最常见的一种离子化学,人们需要处理。这是一个多元阴离子的负电荷2。
我们发现硫酸盐在范围广泛的化合物,一些知名MgSO4, CaSO4 Na2SO4, PbSO4。我们可以很容易地准备硫酸盐通过氧化金属亚硫酸盐和硫化物。我们还可以使用硫酸和金属得到我们需要的硫酸酯盐。
锌+硫酸- - > H2 + ZnSO4(这里我们被用硫酸处理锌金属硫酸锌)。
因为我们可以很容易地得到这些离子,无论是自然或综合,这可以帮助我们在日常生活中在很多方面比你能想到的现在!
从身体和hygiene-care产品像牙膏、洗发水、肥皂、洗涤剂和水处理过程,我们可以发现硫酸化合物的应用无处不在。
虽然可以使用在一些设施,硫酸盐也有其缺点。
它在酸雨中扮演一个重要的因素构成。不仅如此,据推断,硫在冷却效果和间接作用全球变暗。
我们必须了解化学键和附加功能ofSO42——所以,我们有一个清晰的图像,而且知道性质和原子反应。
SO42路易斯结构
作为每一个分子的内部结构,我们知道一个分子是由原子反过来是由原子核和电子组成的。
带负电的电子,粒子,存在于原子核周围的壳。
当我们讨论通过化学键路易斯结构的概念,我们认为最外层的电子即价电子层电子点和原子之间形成的债券为直线。
因此,路易斯结构也称为电子点结构,是一种最主要的和最简单的概念来理解分子化合物的化学键。
在这里,我们将与硫酸盐离子。e SO42 -。
第一步:计算分子中价电子的总数/离子
硫酸盐离子,我们有一个分子的硫和四个氧气分子。
硫和氧都属于同一个组的元素周期表(硫族元素家族)和各有6个价电子。
总价电子SO42 - = 6 * 1 + 6 * 4 + 2 = 32
请注意:我们必须添加两个电子由于硫酸- 2 -电荷离子。
第二步:找出中心原子
找出中心原子的分子,我们必须考虑电负性。
电负性的测量是一个原子的倾向形成阴离子分子吸引带负电荷的电子。
在这里,硫和氧,氧的电负性更强。因此,年代或硫是中心原子。
第三步:画出分子的骨架图
我们现在要素描硫酸盐离子的骨架图的帮助下原子符号和点线结构。

在这里,我们把硫和氧的象征一样每符号,把价电子点。
步骤4:检查八隅体规则
原子在元素周期表的主要群体倾向于有价后八惰性气体氩、氙,等等。
所以,当不同类型的原子分子形式的结合,他们遵循八隅体规则。
在上述图中我们看到,五个分子已经满足八隅体配置和总价电子数是32。通过单键,我们得到的结构为:
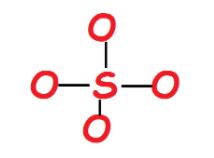
步骤5:形式电荷计算
从上面的示意图,我们可能认为我们已经找到了完美的路易斯结构但有一步离开了。
我们需要计算形式电荷来检查是否所有的组成原子的最可能的形式电荷值。
为此,我们需要使用以下公式:
形式电荷=价电子-孤对电子- 0.5 *保税电子
对于每一个氧原子,形式电荷= 6 - 6 - 0.5 * 2 = 1
硫原子,形式电荷= 6 - 0 - 0.5 * 8 = + 2
我们需要减少的价值形式电荷值。所以,一个单键是不够的。我们需要创建双键。
如果我们考虑在两个双键硫氧组合,我们得到以下结构。
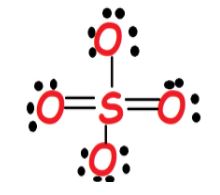
现在,如果我们检查正式指控,我们会发现,硫的形式电荷为零,双重的保税氧原子是零,和单独的保税氧原子是1。
所以,我们在这里得到了完美的路易斯结构!
让我们继续下一个话题:分子几何。
SO42分子几何
一旦我们推导出最好的路易斯结构关系图对于我们给定的分子,我们需要深入调查,找出分子可以在一架飞机!
分子几何给我们详细的知识的三维表示用一块关于原子保税在什么角度。
找出SO42 -的分子形状,我们需要上网VSEPR理论,简称价层电子对排斥的理论。
通过VSEPR模型,我们最小化之间的斥力带负电荷组成原子核周围电子云。
让我们考虑AXN的公式:
在这里,一个代表中心原子,硫磺。
X代表保税硫原子的数量,在4。(四个氧原子周围中央S),孤N代表成键电子的电子。
在这里,如果我们考虑一个X,我们得到的合成公式大举裁员。
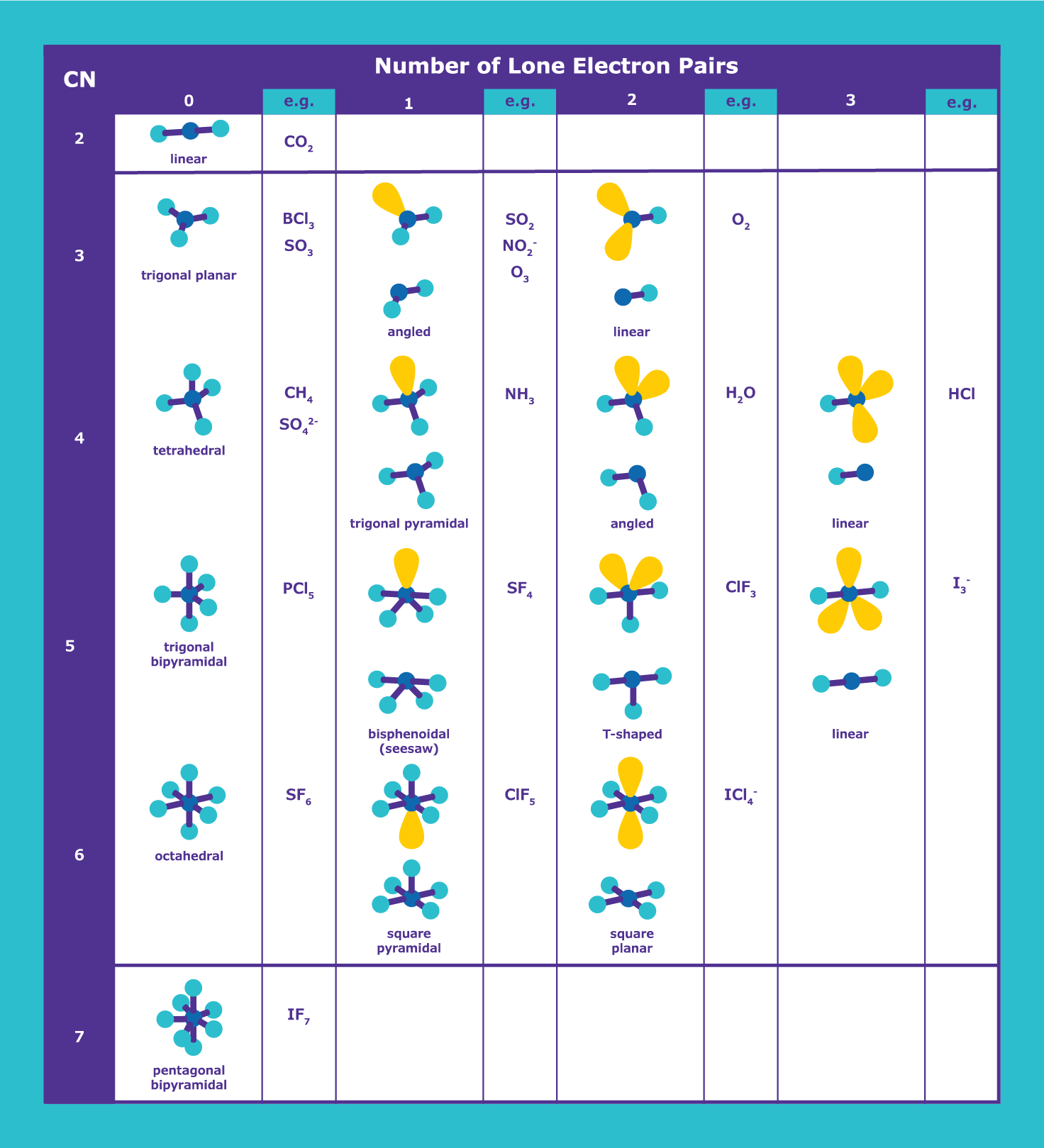
根据图表,我们可以看到,SO42 -有一个四面体结构。键角几乎是大约109.50度。
这是一个精确的分子形状草图在三维空间中硫酸盐离子。
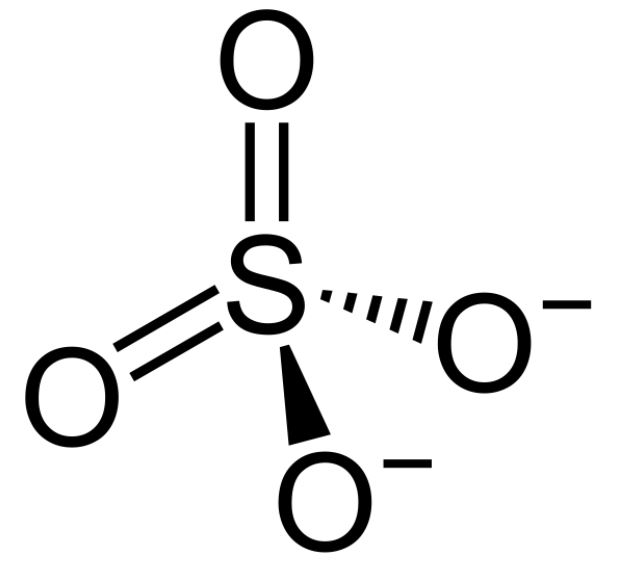
SO42杂交
杂交是一个重要的化学成键的概念,将随时随地方便的东西当我们需要讨论一个分子或了解它的属性。
定义
杂交是类似的能级的原子轨道理论融合,结合形成杂化轨道。我们发现不同的杂交分子像sp, sp2和sp3,根据轨道重叠。
在硫酸盐离子的情况下,我们需要找出杂交理解轨道的重叠。
我们能找到这了一个很简单的公式:
H = 1/2 (V + M + a - c)
在这里,H代表杂交的类型
V代表有关中心原子的价电子的个数
M代表单价原子
A和C代表一个分子的内部存在阴离子和阳离子的指控。
硫酸盐离子、V = 6 M = 0 = 2, C = 0
因此H值是:
H = 0.5 (6 + 0 + 2 - 0) = 4
这代表sp3杂化。
电子配置硫是:
S = 3 s23p4 (Ne)
如果我们扩大我们得到:
S = (Ne) 3 s2 3 px2 3 py1 3 pz1 3 d0
如果我们分开我们,
S = (Ne) 3 s1 px1 3 pz1 py1 3 dxy1 3 dyz1
在这里,s和p轨道结合和融合形成sp3杂化而d轨道保持unhybridized。
SO42极性
定义
极性是处理偶极矩和电负性差异(至少0.5)在一个分子或离子。
这意味着,如果一个复合包含原子具有不同的电负性值。e电子分布不对称,它通常意味着它是极性。里面有部分正负电荷的极性分子(δ+和δ-)。
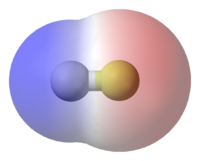
我们通过一个术语称为偶极矩测量极性。
硫酸盐离子的极性
你知道存在共振的SO42 -离子?
硫酸,我们有六个共振结构在图中我们可以看到。
我们已经找到了完美的路易斯结构和分子形状是四面体的检查。
SO42 -,没有波兰人由于结构是对称的。
但这并不意味着没有最终费用,因为我们知道这是一个离子双负电荷。
因此,这种离子往往与其他极性化合物尽管被非极性反应本身。这欠带电分子相互作用的局部电荷存在于任何极性化合物,例如,水(水)。
结论
硫酸盐离子盐自然和工业准备是一个重要的化学成分,我们需要学习。我们会遇到很多化合物在未来将承担硫酸盐离子。所以需要有一些关于它的知识理解可能的反应和相应的化合物的物理和化学性质。化学键能帮助我们得到一个可靠和光滑知道原子组件的本质。
在这篇文章中,我们已经介绍了路易斯结构,极性分子几何,自然杂交类型和SO42 -在一个广泛的格式。这将使你的学习的硫酸盐离子更容易!




