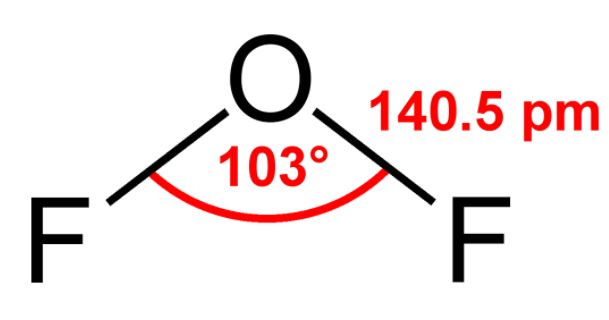
氧二氟化物或OF2化合物之间的反应形成的卤素氟和稀释的氢氧化钠水溶液(氢氧化钠)。
氧二氟化物的制备的方程:
2 f2 + 2氢氧化钠- - > OF2 + 2氟化钠+ H2O
它是一种无色的气体化合物表现出强大的特殊气味和充当氧化剂。它的沸点为128.40 K和49.3 K的熔点。它的摩尔质量53.996克/摩尔和密度为1.88 g / l作为气体在室温下。
尽管它使用强氧化剂,例如,在推进剂的火箭燃料,这个属性也使复合不安全。
OF2可以接触到水和爆炸据说是高度腐蚀性的皮肤。它也可以影响眼睛和心血管系统。
让我们有一个快速但详细观察分子的内部,并讨论其化学键的性质。
OF2路易斯结构
你知道几个因素使原子聚集和结合形成不同的化合物?
当原子聚在一起,与他人建立联系,创建一个新的分子。
通常情况下,一个原子的外层电子,也称为价电子,参与化学成键。
路易斯结构,因此,是一个简单的草图和建设性的过程的图解表示分子的帮助下electron-dot结构。
它给了我们一个2 d图,帮助我们有一个短暂的了解电子安排和债券形成的类型不太多的细节。
现在,我们将讨论形成OF2的路易斯结构的步骤。
步骤形成OF2路易斯结构关系图
步骤1:找到价电子的总数。
首先,也是最重要的一步是计算的总数OF2分子的价电子。
氧气属于集团16日硫族元素家族,化合价的6。氟属于卤素17组的家庭和有价7。
因此,价电子的总数= 6 + 7 * 2 = 20。
步骤2:确定中心原子
现在,我们必须破译中心原子的分子。如果我们看一下鲍林电负性图表,我们可以发现至少负电性元素在氧气和氟氧(O)。
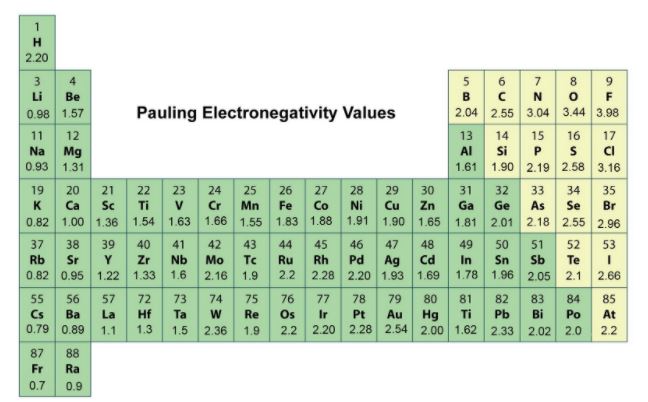
氧二氟化物的中心原子分子氧。
步骤3:分子的骨架图草图
在路易斯结构,我们使用碳原子符号像C, H代表组成原子氢,电子点符号代表价层电子。
让我们看看下面的骨骼草图:
- 原子符号:

- 原子符号还有点符号:
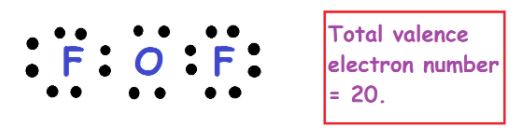
步骤4:八隅体规则
主组(组1组17)的元素周期表倾向于获得的八隅体配置惰性气体元素出现在集团18。这就是所谓的八隅体实现自元素想要达到八个电子的价壳层。
例如,碳倾向于获得一个霓虹灯配置。
例外:氢倾向于实现氦配置,因此只有两个电子外壳。
在这里,如果我们看看八隅体规则,氟原子的化合价八。这同样适用于中央氧原子。
步骤5:形式电荷的概念
在我们继续进行之前,确认任何素描完美的路易斯结构对于一个给定的分子或离子的结构,我们需要检查形式电荷值。

氧气:形式电荷= 6 - 0.5 * 4 - 4 = 6 - 2 - 4 = 0。
对于每一个氟原子:形式电荷= 7 - 0.5 * 2 - 6 = 7 - 1 6 = 0。
因为他们最少的元素存在形式电荷值,我们取得了合适的路易斯结构配置。
让我们来看看:
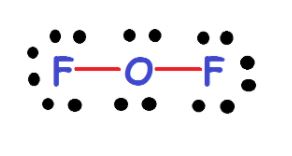
这里,氧气形成单键与每一个氟原子(o f)。
OF2分子几何
我们已经找到了2 d的路易斯结构图二氟化物氧气分子。
现在,我们要破解3 d分子形状。通过路易斯结构,我们已经意识到债券形成的类型和数量的孤独或粘结对价电子在OF2分子。
我们的下一步是使用价层电子对排斥理论(VSEPR)找到确切的分子几何与键角。
创建一个带负电荷的云像带电电子围绕着原子核和排斥。VSEPR模型倾向于减少或减少任何给定的排斥力量和平衡稳定分子,在这种情况下,OF2。
让我们看看这个VSEPR图表显示AXN符号:
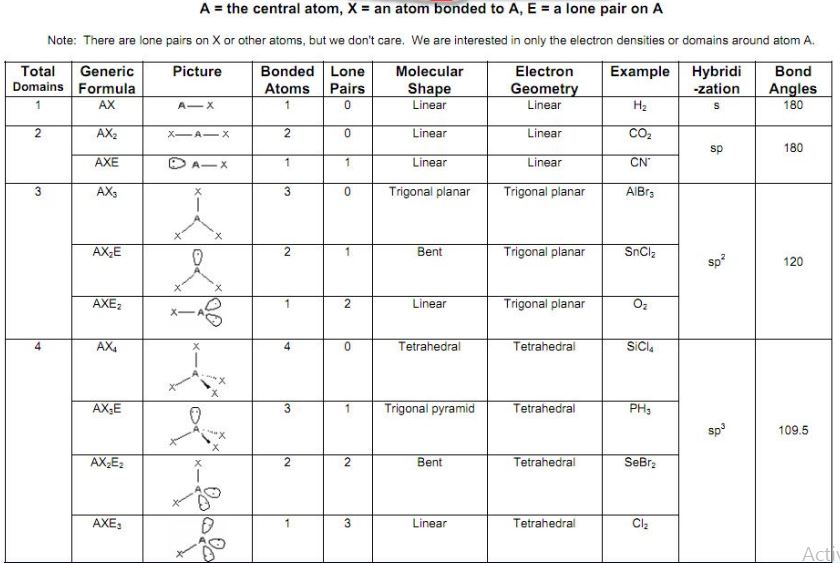
根据AXnEx VSEPR理论的符号,
中心原子(氧气)
X:没有。周围的原子,“n”= 2(氟)
艾凡:没有。中心原子的孤对电子,X = 2。
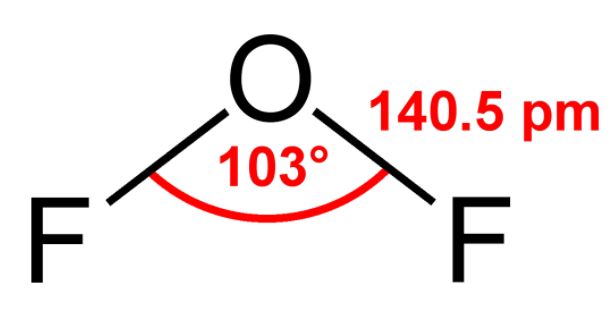
OF2分子是AX2E2 VSEPR符号。根据上面的图表,我们有一个弯曲的分子结构。
键角是103度左右(由于孤对排斥的)。
杂交
在化学中,一个轨道是一个固定的路径原子核周围的电子移动或旋转。定义一个轨道,另一方面,是存在一个电子的概率在任何给定的区域空间。
原子轨道的几个形状像球形,肩部,苜蓿叶或油炸圈饼等等复杂的品种。我们有s、p、d, f原子轨道(代谢)。
电子可以通过波函数在量子力学解释。如果我们考虑到的几个原子轨道波函数,我们遇到杂交的过程。
例如,波函数的年代和2 px轨道产生sp杂交,这常常会导致线性几何。
杂交OF2
让我们看看氧气和氟原子的电子排布基态。
O: 1 s2 2 s2 2 p4
F: 1 s2 2 s2 2 p5
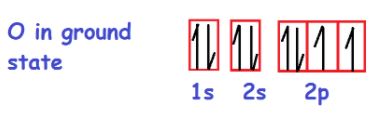
与卤素F和形成债券后达到八隅体配置,O的电子结构是这样的:
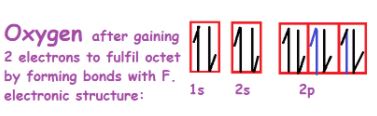
因此,我们在最外层的中央氧原子,四个杂化轨道:2 s, 2 px, 2 py, 2 pz轨道。
空间数量=数量的原子连着中心原子在分子+数量与中心原子的孤对电子
同时,空间数量= 2 + 2 = 4。
因此,我们已经为中央sp3杂化分子的原子氧二氟化物(OF2)。
OF2极性
首先让我们明白我们所说的非常著名的和共同的术语:极性。
极性可以被定义为任何分子的物理性质或化学化合物的组成原子元素可以拥有或正面或负面指控或两者兼而有之。
我们已经看到了鲍林电负性表。主要组的每个元素周期表有一定的电负性的价值。
在相同元素的原子聚集在一起等于比率,电荷值中和自己和净偶极子为零,因此非极性分子。通常线性或对称的化学分子非极性。(例如:H2)
然而,如果分子由不均匀的局部电荷分布由于电负性的差异或分子形状不对称,净偶极子不取消或变成零,我们有一个极性分子。
(例如:有H3PO4盐酸)。
你也可以参考极性的盐酸。
OF2是一个极性分子?
让我们有一个快速氧二氟化物的分子形状。几乎是类似于水和在这两种情况下,中央有两个孤对顶部。
氧的电负性值是3.44。氟是3.98的。
自氧阳性比氟原子,它将拥有部分正电荷(δ+)和每个F原子将拥有消极的部分电荷(δ)。
因此,我们可以看到,有一个电负性差异和今后的净偶极矩不等于零。
再次,OF2不是对称的线性结构。中央氧原子上的孤给它一个弯曲的分子几何类似于英语字母V。
我们已经通过电荷分布不均匀、不对称的氧二氟化物。
分子是极性的性质。
的详细信息,您还必须读文章写的极性的OF2。
OF2分子轨道(MO)图
价电子成键理论对解释化学结合在一个分子结构很重要但它有一些局限性或缺陷。
这里,是分子轨道理论或非常贴切。
在年检中,我们考虑分子轨道的概念(MOs)分子的轨道作为一个整体,而不仅仅是单个原子的组成部分。
它认为电子离域和结果在创建成键和反键轨道的相互作用。
展示的相对能量代谢和合成金属氧化物半导体,我们有分子轨道图。
能量较低的分子轨道的成键和更高的能源是反键轨道。
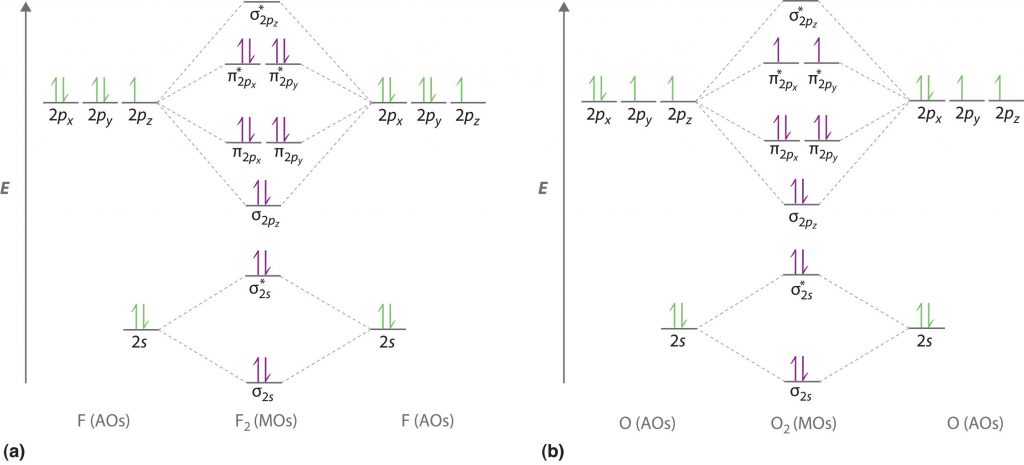
下文提及图表给我们氧气和氟的个人莫图分别OF2的原子组成的分子。
结论
在本文中,我们已经讨论了化学键的类型发生在一个OF2分子。分子氧二氟化物是一个有趣的意外发现的,后来有几个应用程序本质上虽然是有毒的。
我们已经介绍了路易斯结构,VSEPR理论来确定分子几何,杂交,极自然,莫图上简要讨论关于氧二氟化物。
学习快乐!