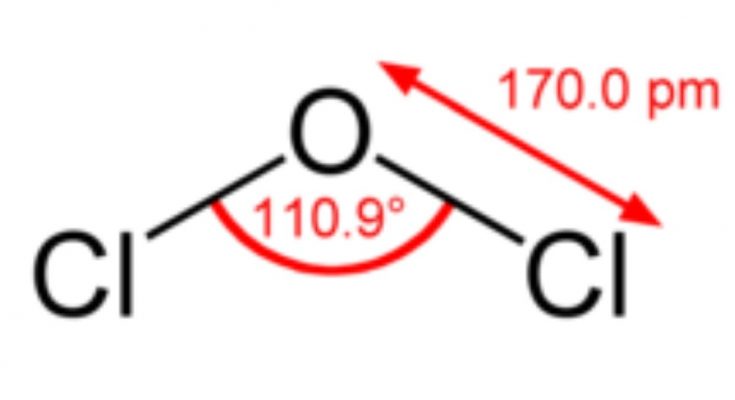
的分子式是OCl2 dichlorine一氧化碳是一种无机化合物现有为褐黄色气体在室温下。dichlorine属于氯氧化家族,溶于水和有机溶剂。
此外,被次氯酸的酸酐,dichlorine一氧化碳是一种强氧化剂和氯化剂。
有不同的方法制备这种化合物在一些下面提到的反应是:
- 2氯+ HgO - - - > HgCl2 + Cl2O
- 2 + 2氯na2co3 + H2O - - > Cl2O + 2 nahco3 + 2氯化钠
2 + 2氯NaHCO3 - - > Cl2O co2 + 2 + 2生理盐水+ H2O
2氯+ Na2CO3 - - - > Cl2O + CO2 + 2氯化钠
准备dichlorine一氧化汞是一种老方法,它不是首选用于商业目的,因为它是昂贵的和具有更高的暴露于汞中毒的危险。
此外,dichlorine一氧化碳被认为是一个主要的爆炸作为室温混合物中氧的存在只能借助电火花爆炸直到OCl2存在23.5%的最低。
价电子和八隅体规则
电子出现在最外层壳被称为价电子,因为它们容易参与债券形成形成新的分子。
价电子只参与债券形成,因为他们从原子的原子核最远的是由于他们没有得到容易受到它的引力。
此外,按照八隅体规则,原子最多可以有8个价电子在最外层,他们只需要这些许多稳定他们的八隅体。8是一个决定的数字,每个原子都想实现惰性气体的电子排布。
然而,许多团体在元素周期表不遵循这条规则最外层可以伸展自己容纳更多的价电子。
路易斯结构的Dichlorine一氧化碳(OCl2)
路易斯点的结构是一个粗略的图解的方法确定参与原子键的形成是如何发生的。
的结构决定了共享价电子发生以及是否一个双键或三键形成。根据这些信息,分子几何、杂交和分子轨道图可以进一步研究。
开始研究一氧化dichlorine的路易斯结构,这是第一次研究参与的路易斯结构化学的关键元素。
氧的原子序数是8,它的电子排布是1 s2 2 s2 2 p4。为了达到稳定状态,p壳需要适应6电子有两个电子的稀缺性使得氧气6个价电子。
另一方面,氯,它的原子序数是17的电子配置是1 s2 2 s2 2 p6 3 s2 3 p5。p壳需要6电子总,有一个短缺的一个电子的总数为氯7个价电子。
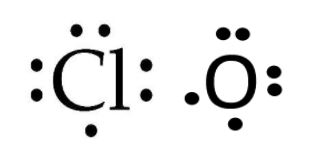
现在,开始画路易斯结构dichlorine一氧化碳(OCl2),我们需要遵循一个循序渐进的方法:
步骤1:总共有多少个价电子已经用于一个OCl2分子?它是20 6来自氧原子和7个来自每个氯分子。
步骤2:需要多少个价电子OCl2分子呢?四个,一个是需要每一个氯原子和两个氧原子所要求的。
步骤3:哪个原子可以在一个OCl2中心原子分子?它将氧气存在一个单一的实体,氯有两个原子。
步骤4:什么类型的债券形成发生在一个OCl2分子?参与原子之间形成一个共价键。
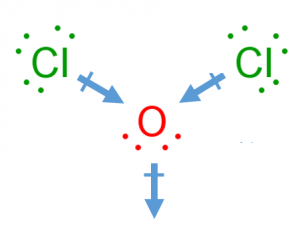
步骤5:现在画的结构组装所有前面提到的点:
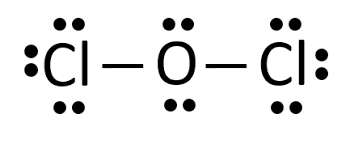
分子几何Dichlorine一氧化碳(OCl2)
分子几何是一个3 d的安排参与分子内原子有助于学习键长,键角和其他几何参数与原子分子有关。
通过分子几何图,一个人可以研究杂交,分子的极性和分子轨道结构确定价电子接受债券的行为的形成。
氧和氯原子之间的键角(O-Cl)是110.9°使分子弯曲或v型。
这可以研究的帮助下价层电子对排斥的理论说,氧原子电负性大于氯由于共享电子接近的氧原子。
此外,这些电子相互靠近而产生排斥的结果增加了角。除此之外,氯原子的大小必须是大于3的氧原子,由孤对电子。
这些电子产生排斥力,所有的氯原子的孤对增加键角。感兴趣的可能是理想的分子形状AX2结构是线性的,V形化合物有AX2E2通用公式。
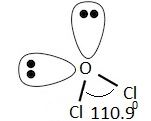
杂交的Dichlorine一氧化碳(OCl2)
杂交是一个数学的过程相同的原子的原子轨道组合产生全新的轨道组成完全不同的组件但是有类似能量的原子轨道。
在这里,重要的是要明白,旧的和新的原子轨道有类似的能量但不等效,任何机会。
OCl2,中心原子,氧气是sp3杂化形式两个氯原子的债券,包括两个孤对电子。所以,总共需要四个杂化轨道所形成的混合1 s轨道和3 p轨道。
因此,四个新形成的杂化轨道有25%和75% p的特点。的杂交OCl2可以详细研究的帮助下价电子成键理论(VBT)说,s轨道比p轨道靠近细胞核和较低的能量,sp3杂化分子的电子非常远离原子核。
我们知道,电子将更稳定的如果他们接近原子核,所以如果有一个负电荷,sp3杂化分子一般不太稳定。
在这里,重要的是要理解,sp3杂化轨道通常产生一个四面体形状的键角近109°。
Dichlorine一氧化碳(OCl2)是一个例外,其分子几何弯曲形状和键角是110.9°的存在主要是由于两个孤对电子,产生排斥改变OCl2分子的完整结构。
极性在Dichlorine一氧化碳(OCl2)
化学,极性导致电荷的分离创造净偶极矩对整个分子有一个带负电,另一个带正电。
这个属性显示主要由共价分子之间共享电子参与分子不捐赠的任何机会。
对于dichlorine一氧化碳(OCl2),这是一个极性分子氧和氯键的偶极矩(O-Cl)不取消彼此留下一个偶极子云。氧的电负性值和氯3.44和3.16,差异是0.28。
这个值不为零,存在一个净一氧化偶极矩使dichlorine极性分子。它可能会让你感兴趣,参与的电负性之差值越低,将极性强度较低的行为,反之亦然。
根据定义,在原子电负性是一个趋势,它吸引了共享电子对本身。所以,电负性数值越高,越强的吸引力的电子原子,反之亦然。
结论
Dichlorine一氧化碳(OCl2)是一种无机化合物,可以在许多不同的方式,但最喜欢的是使用钠作为一个主要组成部分。
OCl2路易斯结构的,很明显,氧气分子有两个孤对电子,改变分子的几何线性弯曲或v型。
此外,OCl2是sp3杂化的这意味着存在四个杂化轨道相似的能量稳定的整体结构的分子。在极性中,OCl2极地一样存在一个偶极矩的净但强度很弱。