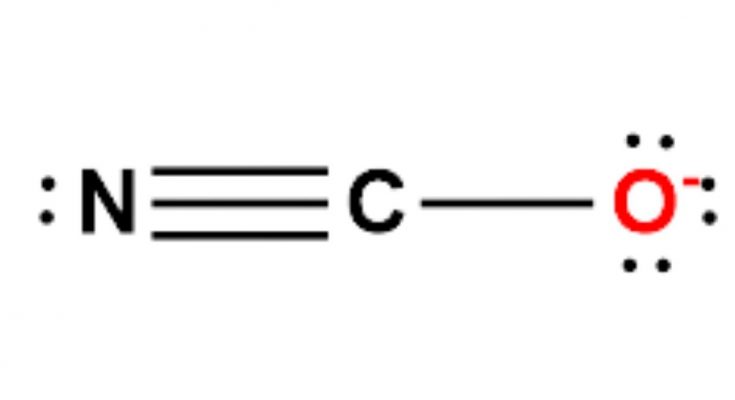
氰酸盐离子是一种带负电荷的实体,用OCN-表示。它有一个结构公式[O=C=N]−。这种离子存在于不同的化合物中,如氰酸铵。氰酸离子起着环境配体的作用。这意味着氰酸盐离子可以与金属离子形成复杂的键,而氮或氧离子可以成为电子供体。
所有三个原子在氰酸盐离子中都在一条直线上,从而形成线性结构。电子结构最好的描述是:Ö̤−C≡N:有一个单一的C - o键和一个三重C≡N键。
在氰酸盐的红外光谱中,在约2096 cm−1处有一个波段。这种高频率导致了这个键是三键的结论。
氰酸盐离子是路易斯碱,因为氮和氧都含有一对孤电子。任何一对孤对都可以被路易斯受体接受。
路易斯结构:氰酸盐离子是路易斯碱,本文进一步强调了其路易斯结构的形成。
几何形状:线性形状
杂交:sp杂交(键角180°)
极性:极性分子
氰酸盐离子的路易斯结构
逐步形成Lewis结构的过程:
把每个原子的价电子数加起来,然后修正一个分子的总电荷数。
写出结构中原子的符号,注意它们的构型。
一般来说,具有最小电负性的化合物的原子将是分子的中心。
用线表示原子间的键,用单独的点表示孤对。
步骤1:碳、氮和氧的原子序数分别是6、7和8。每个原子将满足s轨道的2个电子。剩下的电子会填入p轨道。
因此,碳有四个价电子,氮有五个价电子,氧有六个价电子。
总的来说,我们可以看到在这一步有15个价电子。
考虑到一个额外的电子来自氰酸盐离子上的负电荷,它总共有16个价电子。这也可以用下面的公式来解释:
所需债券数量=(供需)/ 2
为了使每个原子稳定,我们总共需要24个电子。但是,我们总共有16个电子。
24减去16得4。生成氰酸根需要4个键。
以下可以是完成氰酸盐离子电子需求的概率:
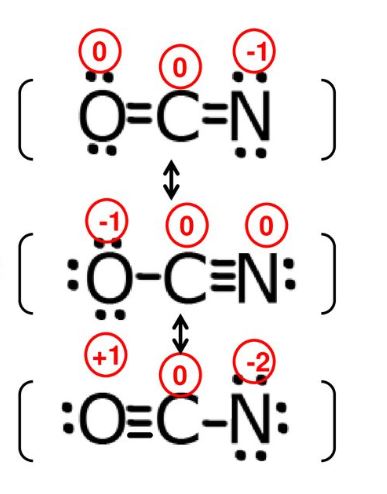
步骤2:碳可以与氮和氧共用两个键,也可以与氮和氧形成三键。每个共振结构都会在不同的原子上带一个负电荷。
为了验证这一点,我们将使用另一个公式:
公式:原子电荷=价电子-(孤电子-键数)
对每个原子分别使用上面的公式,第一个化合物在氮原子上有一个负电荷。
而第二种化合物在氧原子上带负电荷。
上图中描述的第三种共振结构,氧原子带正电荷,氮原子带-2电荷。
以下是预测哪种化合物存在几率最高的条件:
八隅体应该出现
最小电荷分离
电负性最强的原子上是负的F.C
步骤3:综合以上三个条件,我们可以得出结论,上图中氰酸盐离子的第二个共振结构存在概率最大,因为它符合上述所有条件,并且在氧上也有孤对,即;它是电负性最强的原子。
你还得把我写的那篇文章读出来CN路易斯结构.

氰酸盐离子的几何与杂化
方法1
VSEPR理论通过观察中心原子周围的电子和这些原子之间形成的共价键来确定共价键的几何形状。
这个理论依赖于这样一个假设:一个分子通过最小化它在价壳层的电子斥力来达到一个稳定的几何结构。
原子中的电子带负电荷。孤电子对和成键电子对相互排斥,产生静电斥力,将原子推开。
VSEPR理论表明,化合物中的原子总是以一种最小化电子对排斥的方式排列自己。
VESPR理论的假设
1.在由三个或三个以上原子组成的分子中,其中一个原子被认为是中心原子。
2.分子的形状可以由原子中电子的数量以及电子如何相互排斥来决定。
3.两个孤对相互排斥的程度要大于一个孤对和一个键对。
4.中心原子上孤对的存在会导致键角偏离。
5.中心原子和其他原子之间的键的相对强度取决于中心原子和其他原子之间的电负性的差异。
6.三键是指原子共用6个电子,从而产生最大的电子密度。
7.电子对之间的距离越近,它们的斥力就越大,分子的能量也就越高。
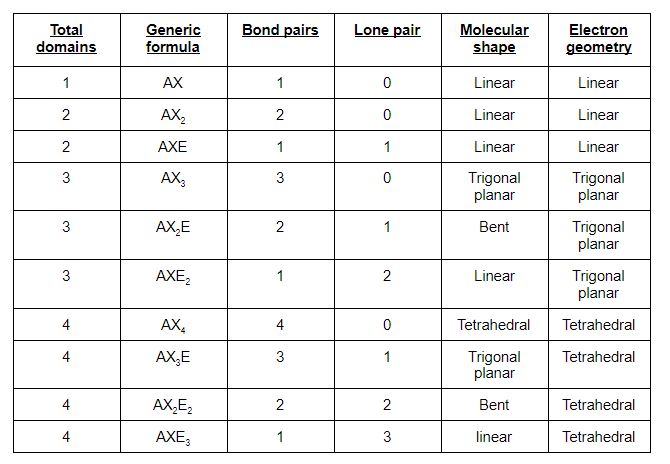
根据上述事实和给定的表格,我们可以说氰酸盐离子的几何将是线性的,它将是sp杂化的。
方法2
在这一阶段,我们对氰酸盐离子Lewis结构的形成已经很熟悉了。
氰酸盐离子与氧共用单键,与氮共用三键。氧在这个离子中带负电荷。
为了找出氰酸盐离子的杂化结构,我们将使用下面的公式:
空间数=(中心原子上孤电子对的数目)+(与中心原子成键的原子数目)
根据上式,氰酸盐离子的空间数-:Ö̤−C≡N:为2。空间位数为2的化合物或离子显示sp杂化。
sp杂化化合物的键角为180°,具有线性几何结构。
氰酸盐离子的极性
极性是衡量分子电荷的标准。
分子的偶极矩平均在0.4到1.7德拜单位之间,称为极性的。氰酸盐离子的偶极矩为1.62207德拜。
根据偶极矩,我们可以看到氰酸盐离子在本质上是极性的。
氰酸盐离子异常
氰酸盐离子,OCN−,有两个活性末端的水分子。这使得形成几种稳定的水合物成为可能。
水连着n端的同分异构体能量总是更稳定。当离子嵌入无定形水中时,O - C和C - N键获得相同的长度。
在水溶液中,氰酸酯通过释放氨的反应转化为碳酸氢盐。虽然这种反应在室温下自发发生,但在分子云的温度下可能非常缓慢或完全不活跃。
但它可能会受到外来能量或温度上升的有利影响,就像扩散星际云的热核或接近近日点的彗星一样。
氰酸盐离子的配体行为
氰酸盐离子表现为环境离子。这意味着氰酸盐离子能够从任何一方开始反应,即。E:来自氧端或氮端。
周围配体的配位模式取决于供体位点和受体的性质。
当考虑含有相同作用的给体原子的配体时,可以看到同样的作用占主导地位。NCO-,其电荷集中在氮上,广泛地与氮配合,而酰胺,与硫酰胺相同的标准形式,与氧配合。
化合物的异构体可以根据其复杂性的几何形状来区分。在n键配合物中,M - NCO单位倾向于线性结构,而o键分子倾向于弯曲结构。
因此,根据x射线晶体学,银氰化络合物具有线性结构。
然而,氰酸银的晶体结构表明,氮原子和银原子以锯齿状链连接。
异氰酸酯是含有官能团−N=C=O的有机化合物。在亲核取代反应中,氰酸酯通常生成异氰酸酯。
异氰酸酯广泛应用于聚氨酯制品和农药的制造;异氰酸甲酯,用于制造杀虫剂。
结论
让我们总结一下本文中关于氰酸盐离子的全部知识。路易斯结构的构成:由于它是阴离子(带电形式),它可以被分解成它的电荷成分,或带负电荷的原子和分子附着在阴离子上。
然后,我们数氰酸酯的价电子数。包括负电荷在内,氰酸酯离子总共有16个价电子。然后我们按照上述方法创建氰酸盐离子的共振结构。
最后,在求出电荷公式后,得到了其正确的路易斯结构和构型。氰酸盐离子是一种' sp '杂化离子。sp杂化离子具有线性结构,键角为180°。它是极性的,因为它的偶极矩远高于零。