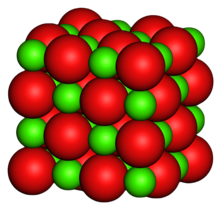
氧化镁(分别)是地球上最丰富的元素之一,存在于岩石的形式如白云石、硅酸盐和镁。此外,氧化镁也出现在海水和生产主要是由菱镁矿煅烧(氧化物)。
除此之外,有许多健康益处的氧化镁,这使得它的最可取的化合物研究的科学家之一。
氧化镁在本质上是吸湿的,这意味着,它携带的能力保留水分子从环境中吸收的帮助下或吸附过程。
因此,在人体氧化镁与水混合生产氢氧化镁,是一个著名的抗酸剂降低酸度。
分别以+ H2O→毫克(OH) 2
此外,在人体氧化镁确保最佳的蠕动活动促进水肿。
消化道蠕动的非随意运动的肌肉产生波状的收缩。这些宫缩开始长反射过程中身体与胃相关联。
氧化镁(分别)是一种白色粉末,燃烧可以创建吸入危害。除此之外,氧化镁(分别)是用于水土修复目的,它可以与废水混合,空气排放处理,饮用水处理,废物处理行业。
价电子是什么?
电子在原子的最外层壳被称为价电子。只有这些电子参与债券形成离原子核最远的和熊最少的吸引力。
由于它,即使一个小景点附近所面临的另一个原子,这些电子激动并接受债券形成产生一个新的分子。
分别以路易斯结构
路易斯结构帮助确定原子的价电子参与债券产生一个分子,最终形成化合物。它是研究通过分析如何在最外层电子(价电子)和它们是如何形成单一,双键和三键。
此外,结构有助于确定一个分子的分子几何形状的原因。由于这个原因,刘易斯图是吸引更多的共价化合物和离子化合物的并不多。
氧化镁是一种离子化合物,失去了价电子和氧镁收到他们达到一个稳定状态。这种行为可以解释通过研究氧化镁的路易斯结构开始分析参与化学元素的原子序数是镁和氧气在这种情况下。
镁的原子序数是12,它的电子排布是1 s2 2 s2 2 p6 3 s2。另一方面,氧的原子序数是8,它的电子排布是1 s2 2 s2 2 p4。
很明显,镁的电子配置有两个价电子而氧有6个价电子。这里,关键是理解,最外层的电子捐赠时少量价电子的存在,许多人都需要稳定的壳。
然而,价电子被接受,当更多的人已经出现,并接受一些满足八隅体。在氧化镁的情况下,氧气已经6个价电子,只需要两个稳定其原子结构,镁捐赠这两个电子的帮助下离子键。
步骤画路易斯结构的氧化镁(分别)
步骤1。找多少个价电子可用在一个氧化镁分子:它是八两个来自镁原子和六个来自氧原子。
步骤2。需要寻找更多的价电子氧化镁分子:只有氧原子需要两个价电子的八隅体镁已经满了。
步骤3。搜索中心原子开始画路易斯结构:不会有共享的电子,不能有任何中心原子。
步骤4。搜索键镁和氧原子之间形成:离子键将原子之间形成的镁将捐赠两个价电子从3 s shell来满足电子缺陷氧原子。
步骤5。现在画路易斯结构的氧化镁(分别):从图中,很明显,镁是阳离子,它有一个2 +正电荷而氧阴离子作为2 -负电荷。
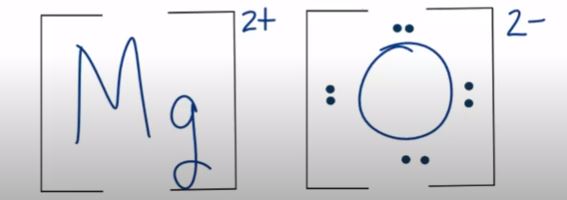
这可能是有趣的意识到镁氧双原子分子中两个原子将被要求用一个氧分子结合,形成两个分子的氧化镁(分别)。
此外,原子的数量或接受捐赠的离子键是一样的参与元素的化合价。
氧化镁(分别)是一个离子化合物吗?
离子化合物时形成一个原子捐赠价电子,另一组不接受他们之间共享的电子参与原子。
这些化合物是由阳离子之间的静电引力(正面)和阴离子(-)离子。
在氧化镁(分别)参与原子都以离子的形式不定向,所以他们不能有分子几何,杂交和分子轨道图。
不符合共价性质和离子结合可以进一步解释的帮助下电负性概念。镁的电负性值是1.2,而氧气是3.5。
作为氧有更高的电负性值,它倾向于把价电子吸引到自己的镁原子倾向于把价电子从其稳定的电子排布。
这就是为什么即使拥有一个稳定的原子结构,镁暴露到更高的能级的氧原子,带走了两个电子从最外层氧稳定。
分子结构的氧化镁(分别)
离子化合物的结构研究几何图形的帮助协调没有方向的说,氧化镁的晶格是紧密结合的八面体形状引起的高熔点。
此外,镁氧化物的晶体结构是岩盐(立方)形状的晶格常数a = 4.212。
协调几何,不是基于方向,研究的价层电子对斥力VSEPR理论不适用。
这意味着协调几何适用于晶格理论目标离子的研究。

氧化镁(分别)极性或非极性吗?
极性的概念仅适用于共价分子的价电子被分享。当电子从镁氧合成化合物,氧化镁不是金属。考虑,极性的概念不适用于氧化镁。
此外,正如有费用发生,镁是阳离子的分离和氧气是一种阴离子,氧化镁可以被认为是一个极性分子。
离子键的氧化镁(分别)——Fajan法则
费根的规则有助于确定bond-forming共价键或离子键。离子键较低的正电荷,大阳离子和阴离子小的情况下氧化镁(分别)。
在分析偏振的力量大阳离子(2 +镁离子),他们的体积被发现了。因此,我们可以得出结论,参与离子的电荷密度低,体积大。
所以,参与离子极化的力量会很低,因为电荷密度很低。这种情况使得氧化镁(分别)分子离子。
现在,当我们分析小离子的极化率(2 -氧离子),他们的有效核电荷的价电子被发现了。随着阴离子中的价电子是松散结合,它们很容易极化两种阴离子和阳离子使氧化镁(分别)更多的离子。
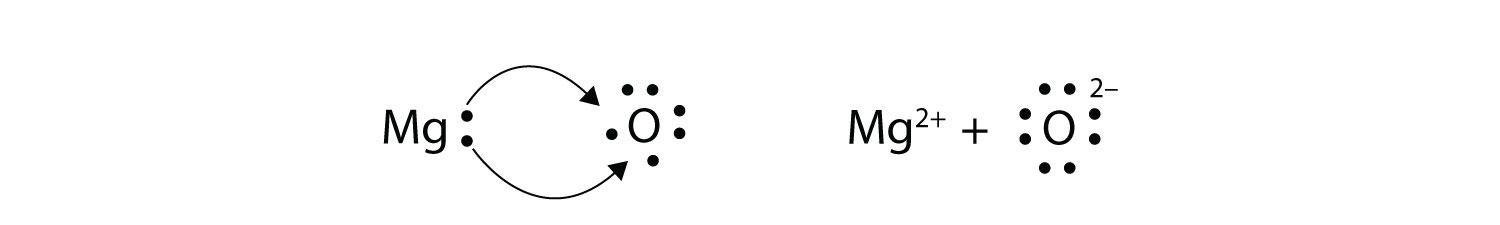
结论
氧化镁是一种非金属离子化合物的形成是因为静电吸引力的力量,没有规则的共价分子,如分子几何、杂交,分子轨道(MO)图,和极性。
可以清楚地看到,镁是一种阳离子有2 +,因为充电2 -氧阴离子。因此,代替分子几何、晶格结构可以在氧化镁研究和分子可以被认为是极性的,尽管房地产只是限于分子共价结合。