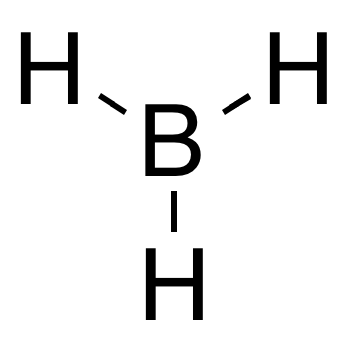
BH3 Trihydridoboron是一种化学化合物在化学公式。它是高活性ie;不稳定的物质。它是一种无色气体。它也被硼烷的名称。许多学生可能会怀疑是否BH3是极性。在这篇文章中,我将回答这个问题并将覆盖其应用程序和属性。
那么,BH3极性或非极性吗?BH3(硼烷)是一种非极性物质,因为对称的三角形平面几何。的电负性硼原子氢(2.04)和(2.20)的几乎是同样的由于b - h键几乎是极性的。也由于对称形状,b - h的极性相互抵消的债券导致非极性分子。
Trihydridoboron存在无色气体。这是一个自然不稳定化合物和高活性。它是不稳定的,因为不完整的硼原子在整个分子的结构。
它可以理解看着硼原子的价电子。在最外层的电子数量是3和硼氢是1。
氢和硼的共价债券即;彼此分享电子。氢和硼原子获得额外的三个电子从原子和填充6最外层电子即;未能完成其八隅体。
因此,这种气体是高度不稳定的分子。因此,硼烷分子二聚得到稳定。下面是二聚在硼烷分子的形象。
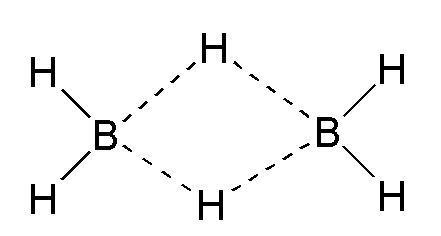
如果我们讨论原子的化学成分和位置,它由3氢原子和1硼原子如上所述,
硼原子的中心原子包围两个氢原子放在三个三角形的角落。H-B-H的键角是120度。
因此,BH3的几何形状是三角形的平面。
硼原子的电负性是氢的2.04和2.20,几乎是相同的。小电负性之差的两个原子形成共价键,小是其极性。
b - h键几乎是极性的。但如果我们把它稍微极地3 b - h键的极性相互抵消了由于对称形状。
因此,BH3 0 D的偶极矩。
极性和非极性分子是什么?
确定是否一个分子是极性,重要的是要检查类型的债券结合分子的力量。
原子间力持有一种物质的分子。离子、共价金属债券、氢键、和许多其他各种类型的债券保持分子束缚的力量。
在所有离子和共价键是最强的。可以极性和非极性共价键取决于分子的几个参数。
极性分子:自然的分子是极性的偶极子是不为零的值。这些分子没有整体等于原子电荷分布。
两个原子形成一个极性共价键如果他们都有不同的电负性。高电负性很高的原子吸引了成键电子对稍微向一边。
由于原子的电负性更高收益部分负电荷和其他原子部分正电荷。这产生两极(积极的和消极的)一个分子。
几个例子这样的分子IF5,甲醇。你可以看看的原因甲醇的极性。
非极性分子:与极性分子,这些分子有一个整体0偶极矩。这些分子中的原子有一个整体的平均分配。
两个原子,形成非极性共价键电负性平等。在这些分子没有波兰人生成。
这些分子的例子有亚兰,PCl5。你可以看看的原因无极性的PCl5。
为什么BH3非极性分子?
Trihydridoboron属于非极性分子的伞,因为它对称的三角形平面形状。
让我们简要讨论。
BH3分子1和3氢硼原子。硼是中心原子,有3个最外层电子被三个氢原子所包围。
单一之间的共价键和氢硼(b - h)形成。所有三个b - h键相互做一个120度角。
硼和氢之间的电负性差异很小(0.16单位),将b - h键因此略有极地。
所有b - h键的极性被相互抵消了由于对称的形状BH3分子。
和偶极矩BH3是0 D。
影响因素的极性分子
的极性分子是由原子的电负性等因素,分子的几何形状和偶极矩。
电负性:一个原子的电负性是它的力量吸引保税电子对向一边。
如果有一个明显的区别两个原子形成共价键的电负性,这种分子的极性增加。
高电负性很高的原子吸引了成键电子对稍微向一边和收益部分负电荷而另一个原子相对正电荷。
这样,创建积极的和消极的波兰人在这样的分子。成正比的极性分子原子的电负性的区别。
偶极矩:一个分子的偶极矩是衡量其极性。更大的价值,更多的是它的极性分子的偶极子。
在数学上,它是费用和中心之间的距离的乘积的正面和负面的。
D = Q * R
非极性分子偶极矩总是0。它用D和SI单位是德拜。
几何形状:一个分子的形状是一个重要的参数检查是否一个分子是极性。
对称的分子形状往往在自然而不对称形状的非极性分子极性的。
同样,对称,BH3是极性分子。
BH3刘易斯和几何结构
Trihydridoboron由3氢和1硼原子。路易斯结构的分子也被称为电子点结构,描述了电子构型的分子。
刘易斯BH3结构类似于BCl3, BF3和其他溴卤化物。
其八隅体Borime原子没有完成。它在最外层有6个电子。
刘易斯Bh3结构,存在只有6个价电子。
三个债券即形成;b - h是一个平面的角120度o彼此。b - h的键长约为119点。
下面是Trihydridoboron的几何结构(BH3)分子。
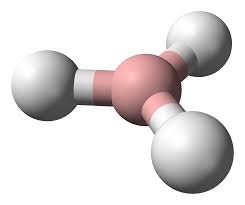
BH3的属性
- 硼烷气体是无色的。
- 因此,在本质上是不稳定的高活性。
- 其分子质量大约是13.83 g·摩尔−1。
- Boronium离子被认为是它的共轭酸。
- 硼氢化阴离子是它的共轭碱。
- BH3的分子的几何形状是三角形的平面。
利用BH3
- 硼氢化合物广泛用于合成各种有机化合物。
- 硼烷羰基BH3 (CO)由硼烷也用于探索硼烷的化学化合物。
结论
硼烷气体分子由一个单一的硼原子包围三个氢原子。三个债券形成的三角形平面形状,因此,形成一个对称的几何图形。
和氢硼原子的电负性之间的差异很小。因此,b - h键稍微极地。
b - h键的极性被相互抵消了由于对称分子的形状。
因此,整个BH3分子的偶极矩是零。
由于这些原因,BH3是极性的。
所以伙计们,如果你有任何疑问关于一样的,你可以问他们在评论部分。我们将尽快联系你。