乙腈,也称为乙腈是一种无色有机液体芳香气味。这是主要的生产在生产丙烯腈作为副产品。用于有机合成的化合物,它充当一个极性非质子溶剂。
这是在1847年首次由Jean Baptiste杜马斯。这也是一个有效的空气污染物中发现汽车和工业尾气。
在本文中,我们将研究CH3CN的路易斯结构及其几何、杂交和极性。读到最后。
CH3CN路易斯结构
路易斯点符号或路易斯结构的图展示不同原子间的成键的化合物,指定数量的债券以及孤对电子。
这些结构考虑中的价电子的所有原子的化合物。这个概念,吉尔伯特·n·刘易斯,推出了1916年。
图是象征和使用化学元素的符号来表示他们的原子而图中的圆点象征的孤对电子与原子连接。
我们已经知道,在一个原子中,电子围绕原子核的明确的轨道称为壳。
八隅体规则
壳离原子核最远的被称为价电子层,这是原子的最外层轨道,电子位于这个壳被称为价电子。
假设一个原子倾向于形成债券为了达到稳定。另外,原子是最稳定的八个原子的价层电子,这就是所谓的八隅体规则。
这条规则的想法来自于电子配置最稳定的惰性气体元素的整个周期表和包含八个电子在最外层,除了氦两个电子。
因此,原子键来完成他们的八隅体导致不同化合物的形成。
CH的路易斯结构3CN给出:

它是可见的在上面,所有参与的八隅体原子结构是满足。因此,正确的路易斯结构。
CH3CN步骤画路易斯结构
现在让我们试着理解制作的路易斯结构通过一个循序渐进的过程。
•画路易斯结构的化合物,我们必须首先计算价电子的总数增加了所有参与原子的价电子。
在CH3CN:
价电子的碳的数量= 4
两个碳原子存在,4 X 2 = 8
同时,氢的价电子数量= 1
三个氢原子1 X 3 = 3
最后,价电子数氮= 5
因此,在CH价电子的总数3CN = 8 + 3 + 5
= 16
•下一步是选择的中心原子的分子。
通常,至少形成了中心原子的电负性物种,在CH3CN,碳是最电负性因此,任何两个碳原子可以选为中心原子和放置在所有其他的分子的中心原子被假定为绑定。
•现在,所有的原子分子的保税的帮助下单键。
这个步骤使我们能够估计的电子数量仍需要的一个或多个原子分子来完成他们的八隅体。

•以上所有氢原子的结构表明,八隅体以及第一个碳原子是满意。
然而,碳原子的行为为中心原子,碳、氮原子仍然需要两个电子来完成他们的八隅体。
•作为碳和氮能够形成多个键第二个碳原子和氮原子形成一个三键,因此,满足八隅体分子中所有原子。
同样,一个孤对电子与氮原子离开。最后的乙腈的路易斯结构是这样的:

•但是,等等,我们如何知道我们画的结构是正确的吗?
以确保我们得到正确的分子结构有另一个概念叫形式电荷。
这是一个理论概念按照所有的形式电荷的原子分子分别计算和图是正确的如果形式电荷的价值接近零或更好的零本身。
•一个原子的形式电荷是使用以下公式计算:
形式电荷=(总没有。价电子的自由州]-[总没有。孤对电子的电子- 1/2(总没有。结合e- - - - - -)]
•现在,计算不同原子的形式电荷CH3CN:
碳原子,形式电荷= [4]- [0]½[8]
= 0
对于氢原子,形式电荷= [1]- [0]½[2]
= 0
氮原子,形式电荷= [5]- [2]½[6]
= 0
,形式电荷的原子是0时单独计算,CH的总电荷3CN也变成了0指示这是最好的路易斯结构的分子。
CH3CN分子几何

一种化合物的分子几何是原子的空间排列。
原子的三维定位,确定化合物的成键和非成键电子出现在中心原子。
分子几何还考虑其他因素,例如债券角度,结合强度等。
价层电子对斥力(VSEPR)理论提供了确定的假设任何化合物的分子几何。
我们已经知道所有的电子带负电荷,同种电荷互相排斥。
因此,一个分子内电子排斥相互远离。根据VSEPR理论,任何分子的三维结构是由这些inter-electronic排斥力量分子内部的工作。
这些力量之间最大的pair-lone对这些电子在空间自由移动,而这种对债券之间的最小。
VSEPR理论进一步指出,电子在分子倾向于定位尽可能避免inter-electronic排斥来自其他电子,因此,尽量减少的能量分子,使其稳定。
分子的路易斯结构有助于我们确定债券的数量对,孤在分子。
按CH的路易斯结构3CN画在前面的部分碳的中心原子的分子。
有两个碳原子在这个分子,它可能有两个不同的形状取决于碳原子选为中心原子。
再看CH的路易斯结构3CN:

•如果C1是选为CH的中心原子分子几何3CN是四面体的中心原子连接到四个不同的基团viz.三个氢原子和一个CN组。
考虑到AXN符号,这种结构类似于斧头4公式,一个是中心原子和X象征着保税集团。
N在孤的符号是指数量上的中心原子CH = 03CN分子。
在这种情况下,电子分子的几何形状也四面体和不同原子之间的键角是109.5°。
然而,如果C2被选为中心原子的分子几何CH3CN分子应该是线性的中心原子与两组viz.一个甲基(ch3)和一个氮。
这类似于斧头2AXN的公式符号。分子的电子几何也是线性键角为180°。
AXN符号图表给出了不同的通用公式如下:

CH3CN杂交
杂化轨道的形成的过程,由于混合轨道有类似的能量水平称为杂交。
任何分子的杂化是由计算分子的空间数量。
根据VSEPR理论,经过数字是中心原子成键原子的数量随着孤。
它是由公式给出:
空间没有。=中心原子的西格玛(σ)债券数量+孤对中心原子
正如前面所讨论的CH3CN分子的碳原子可以被选为中心原子,因此,这个分子有两个杂交状态。

•如果C1选为中心原子,立体号码= 4 + 0 = 4
因此,这个分子变得sp3杂化。
然而,如果C2选为中心原子,立体数= 2 + 0 = 2
因此,分子的杂化成为sp。
下面的图表描述了空间数量之间的关系和杂交状态:
| 位的数量 | 杂化状态 |
| 1 | 年代 |
| 2 | Sp |
| 3 | Sp² |
| 4 | Sp³ |
| 5 | Sp³d |
| 6 | Sp³d² |
CH3CN极性
极性分子中存在两种截然相反的两极即积极的和消极的。
这些两极发展由于之间成键原子的电负性的差异,对本身更多电负性很高的原子吸引电子,因此开发一个微小的负电荷,而另一个原子获得一个轻微的正电荷。

乙腈分子是极性由于碳和氮原子的电负性的差异,由于一个微小的负电荷发生在氮而轻微的碳原子上的正电荷。
CH的偶极矩3CN是3.5德拜。

CH3CN属性
CH的一些重要特性3CN给出下表:
| 化学名称 | 乙腈 |
| 化学公式 | CH3CN |
| 分子量 | 41.053克/摩尔 |
| 沸点 | 在81 - 83°C |
| 熔点 | -46 & - 44°C之间 |
CH3CN使用
CH3CN是使用:
•作为溶剂在丁二烯的净化。
•高效液相色谱法。
•在制备DNA寡核苷酸。
结论
•CH的路易斯结构3CN是:
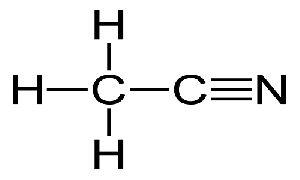
•由于两个碳原子的存在两个不同的分子几何图形CH3CN如果C1选为中央四面体,如果C原子形状2被选为中心原子形状是线性的。
•类似于分子的几何形状有两种杂交的CH3CN分子。
与C1原子作为中心原子杂化状态是sp3而如果C2充当中心原子的杂化状态分子成为sp。
•CH的偶极矩3CN分子3.5德拜。
快乐学习! !




