氯甲烷或CH3CL高活性和易燃的卤代烷化合物。有趣的是,它已经被研究人员研究了空气中氯甲烷的平均寿命是十个月,在此时间段内到达平流层很容易。
每年大约2 x 106吨氯甲烷到达平流层几乎每年总额的25%氯释放。
氯甲烷对环境是有害的,因为它与各种自然下沉到混合所有的土地、空气和水生态系统。氯甲烷是一种稳定的分子,但在高浓度和不断变化的气候模式有什么致命的一个完全处理。
路易斯结构的氯甲烷(CH3Cl)
路易斯结构是一个图示显示了电子在一个原子的价电子层。所绘制的图来确定不同原子的价电子参与债券形成形成一个分子。
在图中,“点”附近一个元素代表了价电子的象征。如果你意识到,这些价电子总是写在对每一方的符号显示如果所有成对的电子存在。
此外,路易斯结构也决定一个单,双或三键之间形成相互作用的原子。
如何画路易斯结构CH3Cl ?
首先CH3Cl的路易斯结构,首先,我们需要确定每个参与原子的电子排布。
氢的原子序数(H)是1,所以它的电子排布是1 s1。随着年代壳需要两个电子,有一个空缺的一个电子,所以价电子的数量在一个原子氢(H)是1。
在碳(C)的情况下,它的原子序数是6,所以电子配置是1 s2 2 s2 2 p2。这使价电子的数量在一个碳(C) 4。
最后对氯(Cl),其电子的原子序数是17配置是1 s2 2 s2 2 p6 3 s2 3 p5。所以,在最外层价电子氯(Cl) 7。
现在,让我们学习的循序渐进的方法画路易斯结构的氯甲烷(CH3Cl)。
步骤1:找到中心原子:单原子电负性最少的通常,变成了中心原子。CH3Cl而言,只有两个单个原子C和Cl,其电负性值是2.6和3.2。随着碳(C)原子有一个较低的值,这将是中心原子。
步骤2:找出参与价电子的总数:这将是想通过添加所有原子的价电子。对于CH3Cl,价电子的总数将14。
步骤3:算出需要多少更多的电子稳定一个CH3Cl分子:一个CH3Cl分子完全更需要八电子稳定结构。
步骤4的数量和类型:寻找bond-forming CH3Cl分子:在CH3Cl的情况下,只有单原子之间形成共价键参与。
步骤5:现在画路易斯图组装上述步骤。

或

分子几何CH3Cl
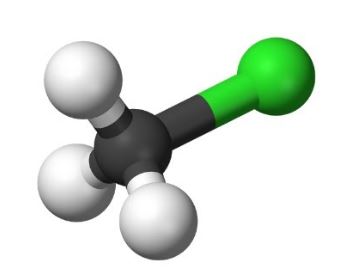
CH3Cl是五原子分子键角为109.5°使分子弯曲形状。
可以研究分子的分子几何的帮助下价层电子对斥力(VSEPR)理论说氯甲烷(CH3Cl)具有四面体形状的键角与碳(C)是109.5°,总是为中心原子。
此外,没有扭曲的结构是没有孤对CH3Cl分子因为每个键是相等的角距离彼此平等出席所有单键导致斥力相等。
下面的3 d表示CH3Cl分子。看一看!
氯甲烷(CH3Cl)极性或非极性吗?
极性分子是那些两个参与原子电负性差异巨大,导致分离的指控。
因此,一端保留一个正电荷,而另一个获得一个负电荷。另一方面,非极性分子那些参与分子之间的电负性差异不大,几乎可以忽略不计。
这并不是导致电荷分离和分子仍处于稳定状态,没有打算与其他附近的原子键,在正常情况下。
找出这个问题的答案,重要的是要确定和比较所有参与原子的电负性值。对于碳(C)和氯原子(Cl)、Cl(3.2)的电负性比C(2.6)所以偶极子的行为从向下向上的方向。
此外,氢的电负性值(2.20)和碳是如此之近,他们的区别是微不足道的使·hc·邦德非极性。但是,整个CH3Cl C-Cl债券是极性,分子携带净极性分子偶极矩。
C-Cl之间的电负性移动向上方向键使CH3Cl分子极性的。
你也应该一旦读了写在专门的文章极性的CH3Cl。
CH3Cl杂交
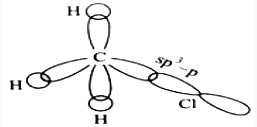
杂交是一种概念,表示不同的化学元素的原子轨道,混合和混和彼此产生新的混合分子影响分子几何和化学分子的成键性质。
细节关于这个可以研究的帮助下了解中心原子的价电子成键理论中一个分子进行杂交sp, sp2, sp3等等。
中心原子的杂化。在CH3Cl分子sp3碳。这是因为CH3Cl分子有四个单键和孤对电子。
当我们讨论发现的杂交分子,我们总是把远离原子核的壳。在碳的情况下,这些贝壳2 s2和2 p2成对电子将首先填2 s shell然后2 px和2 py。
但这种情况不可能四个单键需要适应所有的2 s, 2 px, 2 py, 2 pz贝壳。
为此,每个电子其中杂交和填充所有的2 s, 2 px, 2 py, 2 pz壳提供四个单键填充空间的机会。
这使得中央碳原子sp3杂化三个氢原子在哪里s-sp3杂化和sp3-p单氯原子杂化。
CH3Cl分子轨道图
的分子轨道图是一种图形表示分子中化学键发生,符合规则的分子轨道理论和原子轨道的线性组合。
绘制分子轨道图背后的想法是,一些原子轨道组合形成新的分子轨道,但在相同的数量。
在这里,参与电子往往自己重新分配到不同的轨道杂化轨道。
分子轨道图的主要目的是确定参与轨道的能级和比较他们找出结合发生在一个分子。

对于一个单键,只有σ键(σ)是目前没有π(π)债券。上述图表显示杂交发生在一个分子一个分子提供一个原因决定结合另一个。
碳和氢的原子有几乎相同的电负性值往往以类似的方式,甚至当谈到各自的轨道的能级。
然而,碳和氯有更大的区别它们的电负性值往往会使不同大小的叶表现突出的差异在他们的能级。
结论
氯甲烷(CH3Cl)是一种稳定的化合物的原子在病情稳定,不容易与其他元素反应在正常情况下。路易斯结构可以帮助预测分子的几何、杂交,极性,CH3Cl分子的分子轨道图。
因为CH3Cl分子是高度稳定的,没有变形的结构,分子是一种最简单的Penta-atomic结构研究和学习如何预测不同能级的轨道的帮助下一个分子轨道图。




