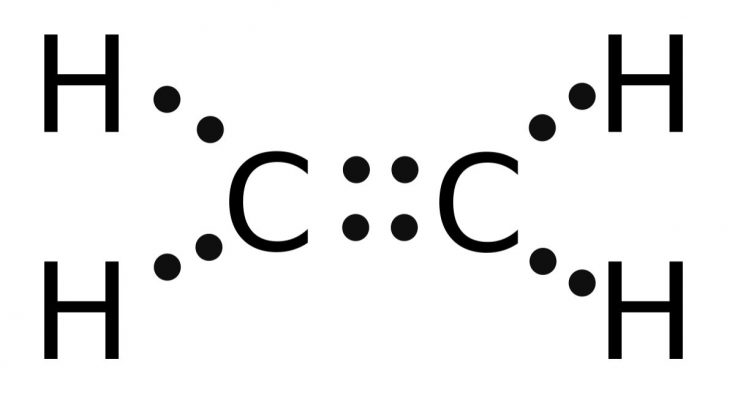碳氢化合物形成一个科学的化学的重要和不可分割的部分。无论是石油、原油或天然气,大多数的这些化石燃料的碳氢化合物在自然。除此之外,我们可以发现它们在合成聚合物和其他人造塑料材料。
他们在本质上是有机的,顾名思义,他们只形成的碳和氢。有时,它还创建了与其他品种,如硫化合物,氮,等等。
虽然这些都是一些简单的有机化合物可以遇到,他们有不同的范围和在许多物理和化学性质都有所不同。
乙烯/乙烯
在本文中,我们将谈论的一个最常见的和广泛使用的碳氢化合物:乙烯(C2H4)。
你知道这种化合物甚至比空气轻吗?
C2H4是一个简单的直链烃,熊甜香味,一种无色。
每当我们读过关于有机化学,我们遇到过这种化合物,是吧?
所以,对我们来说是很重要的学习C2H4详细了解直链烃类的本质在一个更好的方式。
化学键的碳氢化合物
碳与氢自然共价成键时,这导致不同类型的形成我们看到的碳氢化合物。
从简单的甲烷和苯的一些复杂的天然橡胶,在日常生活中我们处理几个高碳钢。
在有机化学中,我们发现碳氢化合物的几种类型:直链,循环,甚至分支。
直链的主要和最容易破译集团碳氢化合物。在这里,我们有:
- 饱和烃:饱和烃也称为单极直链烷烃遵循结构H - (CH2) n。它们发生在形成单键。例子是甲烷和乙烷。
- 不饱和碳氢化合物:这些形成双键和三键和相应的烯烃和炔烃。例子是乙炔和乙烯。
化学结合乙烯
你可曾想过独特而大大不同的宇宙是怎样?
整个宇宙是如何建立由几个原子?
现在,原子通常不存在于自己的在一个孤立的国家,所有我们周围基本上是由原子相互结合形成分子。
根据原子的性质和他们倾向于吸引还是排斥类似或不同的另一个原子,得到合成分子化合物。
这整个过程的两个或两个以上的原子紧密并决定在一起称为化学键。
现在来乙烯,如果我们想要在全面了解它,我们需要做的是理解其键的性质。
对于碳氢键,这在本质上是共价。继续,让我们一步一步地讨论这个问题。
C2H4路易斯结构
电子点结构,广泛被称为路易斯结构,是一个骨骼的图解表示考虑组成原子和分子价电子层电子。
在我们直接到这个之前,我们想把你介绍给(或假设刷你了如果你已经熟悉的)一些非常重要的概念,将使你了解乙烯粘结方式更容易!
价电子
一个原子有核,周围都是带负电荷的电子存在于不同层次或外壳。
最外层被称为价电子层和电子壳层中被称为价电子。
原子的价电子数等于其化合价反过来决定了给定原子的结合能力。
八隅体规则
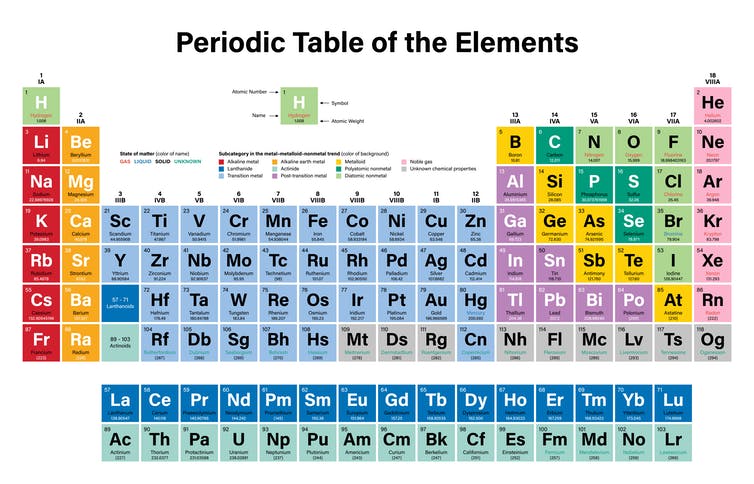
看一看周期表。如果我们看到最后一组,我们可以发现所有的元素是惰性气体在他们八个电子价壳(他有两个除外)。
原子的主要群体倾向于获得更多的电子获得相同的八价。这就是所谓的八隅体规则或八隅体实现。
C2H4路易斯结构的步骤
路易斯结构的分子可以很容易地做如果我们遵循一定的程序。
C2H4是一种不饱和烯烃。
让我们看看我们如何进行:
步骤1:我们有多少原子在一个乙烯分子?
2碳和4氢。
氢是第一个元素周期表,因此只有一个价电子。
在碳的情况下,我们有四个价电子。
∴价电子的总数在C2H4分子之一
= 2 * 4 + 1 * 4 = 12。
步骤2:现在,我们已经发现总价数,我们要检查哪个原子的电负性较小。
对于碳氢化合物,我们总是会把碳中心。氢原子是需要外部头寸。
步骤3:现在,我们绘制了原子的符号,让我们表示点的价电子。
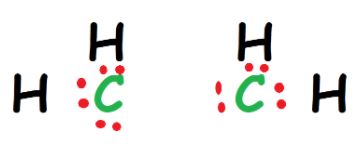
在这里,我们可以看到,一个碳原子的八隅体实现(前八隅体规则讨论)。但是,其他中央碳原子缺少两个电子。
所以,我们能做的是,我们可以把这些电子从底部和地点在两个C原子之间的中心。
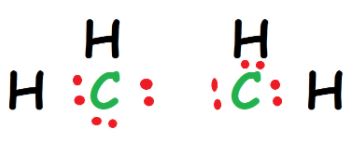
步骤4:我们完成了八隅体实现的概念。这里有两个债券形成以来,我们将有一个双键结构。因此,C2H4烯烃。
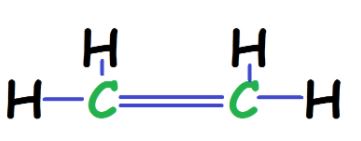
在这里,我们有最合适的乙烯和适当的路易斯结构草图。
分子几何
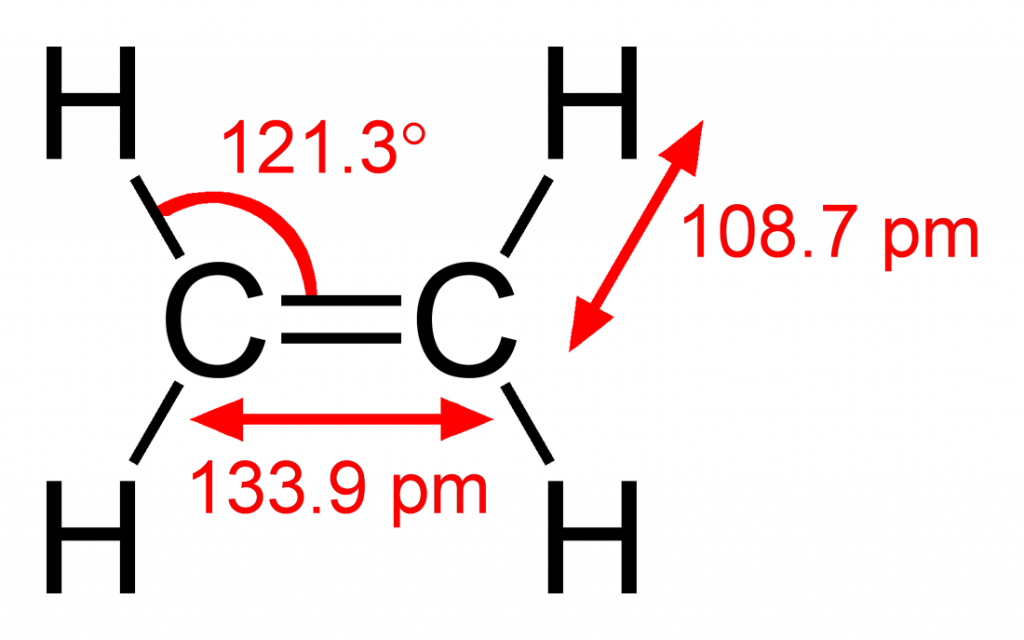
当我们画C2H4的路易斯结构,我们找到一个线性二维表示。在现实中,乙烯的分子形状并不是线性的。
理解化学键,只画路易斯结构图是不够的。我们需要关注分子几何。
分子几何提供了清晰的内部原子化学分子通过提供一个三维的观点。
不仅如此,我们了解其他重要细节键角和长度。
C2H4,我们已经知道,一个烯烃即碳氢化合物有一个双键。
看看VSEPR理论,我们将利用破译分子几何。
VSEPR
VSEPR代表价层电子对排斥模型或理论。同种电荷相互排斥。所以,价电子被带负电荷的分子中有互相排斥的倾向。
VSEPR理论解释了形状通过最小化电子斥力。在这里,我们需要处理的或非共享和保税对电子。
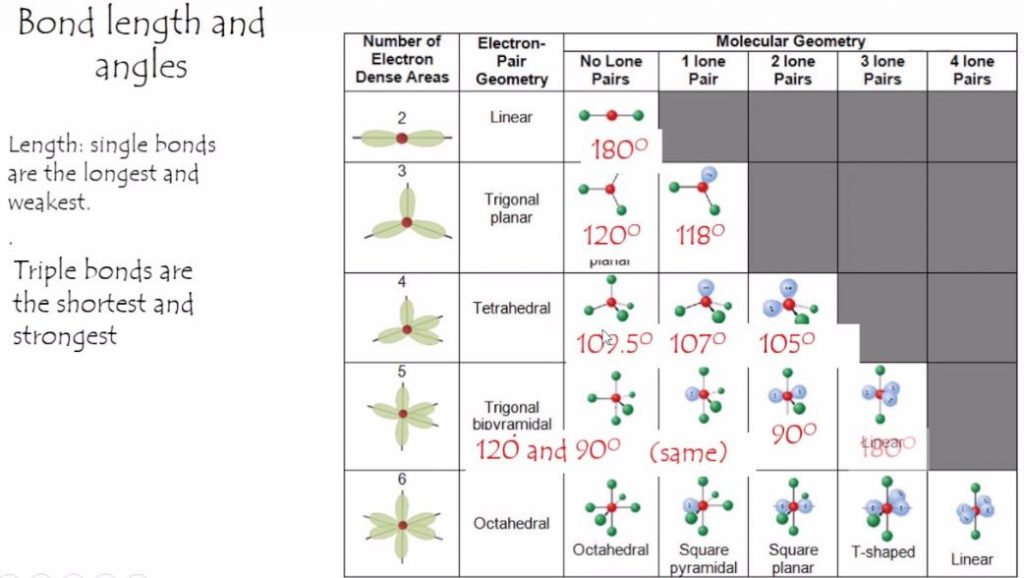
对于C2H4
在C2H4,如果我们的路易斯结构,我们会发现有三个保税对孤对电子在碳和零。
根据VSEPR图表,乙烯分子的形状是三角形的平面。有两个三角形重叠的图中我们可以看到彼此。这是由于这样的事实:每个碳包围着一个平面三角形。
键角是120度左右。
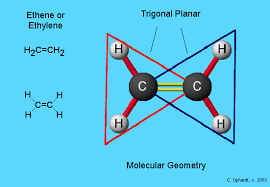
C2H4杂交
原子轨道组合在一起形成杂化轨道和过程称为杂交。
首先,我们需要调查同时发现的杂交分子是原子的电子排布。
C: 1 s2 2 s2 2 p2
H: 1 s1
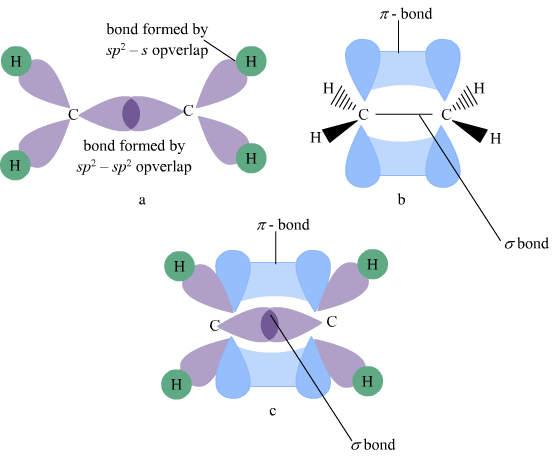
在一个双键,我们有一个σ和一个π键。在一个键,我们有一个sigma键。所以,C2H4,两个sp2杂化轨道,一起从一个碳原子结合形成σ键。
此外,2 p轨道(unhybridized 2 py或2 pz)的两个碳原子结合形成π键。这给了我们的双重(=)债券C = C。
其他sp2杂化轨道之间形成σ键C和H,因此,导致碳氢键一键结构。
C2H4分子轨道(MO)图
分子轨道理论是量子力学的一个概念,在原子线性结合形成分子轨道和我们描述波原子粒子的性质。
这里,键的强度取决于重叠程度反过来取决于原子相结合的空间距离。
σ轨道重叠:这意味着结束交互。
π轨道重叠并排:这表示方法。
类型的轨道:我们处理三个主要类型的轨道成键,非键和反键轨道。
如果我们只考虑π键,我们可以看到unhybridized 2 p轨道(正如前面所讨论的杂交)现在将形成MO -成键和反键轨道。
The bonding orbital will see higher electron density which will hold the atoms together via nuclei attraction.
反键*轨道电子密度将看到一个更大的距离,因此,债券,导致斥力减弱。
CC代表最高占据分子轨道或人类。
CC *代表LUMO(最低未占据分子轨道)。(反键轨道仍然是空的)。
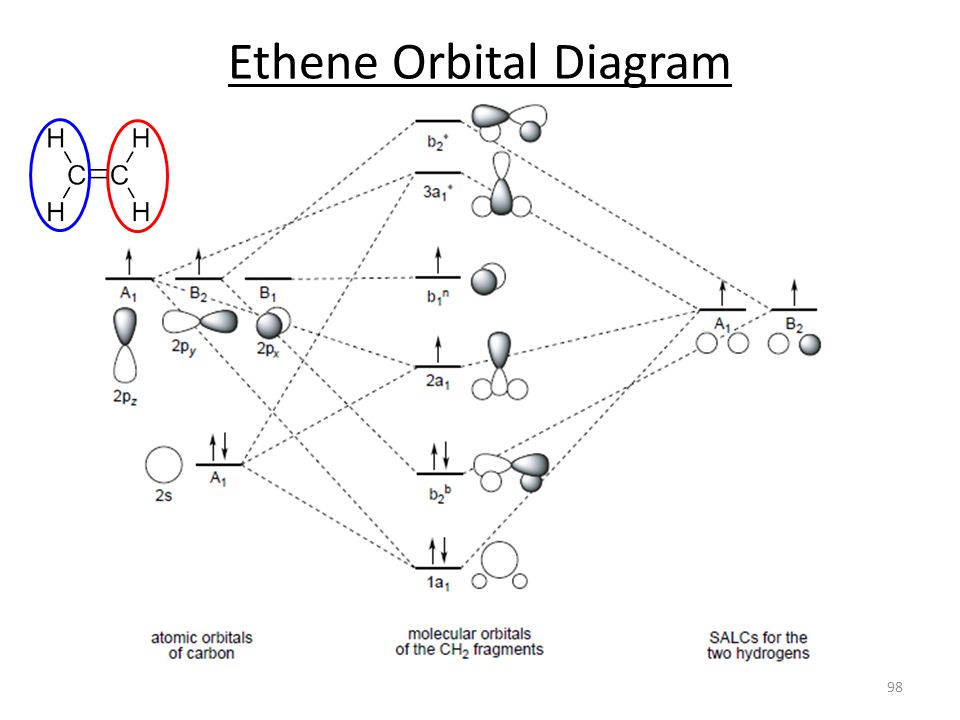
上面的图显示了分子轨道(MO)图的乙烯/乙烯。
极性的C2H4
C2H4分子非极性本质上是所有的原子都是对称排列在分子和碳原子有相同的影响保税电子。
分子均匀电荷分布跨越它,因此分子的偶极矩也变成了零。
更具体的关于C2H4极性的原因,你必须看看这篇文章写在极性的C2H4。
下面是关于C2H4画路易斯结构的视频。看一看
结论
乙烯或C2H4是一种常见的直链无环烯烃和有机碳氢化合物的一个重要成员。有一个双C = C键,它是不饱和,这引起了一些属性。
在这里,我们了解了如何绘制正确的路易斯结构,找出一个乙烯分子的分子几何。此外,我们讨论了其杂交,还提到了分子轨道的概念。
简而言之,我们已经介绍了乙烯的成键性质。
感谢您的阅读!