氧化铝或氧化铝(III)通常被称为氧化铝。在自然界中,它发生在矿物刚玉晶体多态相α-氧化铝。
这是一个两性物质即它能像一个酸以及一个基地。这是一个发现铝的双原子分子离子物质。
在本文中,我们将研究这个分子以及其化学成键原子的帮助下路易斯结构。
除了它之外,我们还将检查它的几何、极性和杂交的氧化铝。所以,让我们开始吧。
路易斯结构的氧化铝
路易斯结构的概念被吉尔伯特·n·刘易斯在1916年首次引入。它也被称为路易斯点图或电子点结构。
的结构说明的位置价电子,参与化学键的形成,在一个分子内的原子。
点邻近的原子代表他们的价电子。路易斯结构描述了最好的位置或安排的电子。
氧化铝是一种离子化合物即铝和氧原子形成间的关系通过电子从一个原子的转移到另一个原子。
路易斯结构的氧化铝(氧化铝)被表示为:

在上面的结构中,可以看出,铝原子被捐赠三个电子而稳定的氧原子完成八隅体接受两个电子。
步骤画路易斯结构的氧化铝
步骤1:画路易斯结构的氧化铝分子我们首先要明白氧原子之间的债券和铝原子。
铝金属,而氧气是一种非金属因此这两个原子之间的键是离子,因此这种化合物的路易斯结构,与共价化合物,说明这两个点(即电子)的帮助下以及不同原子的电荷。
步骤2:现在让我们看看在这个分子的价电子层电子礼物。
13元素和铝是一组有三个原子的价层电子,而氧气是一组16个元素和有六个原子的价层电子。
步骤3:随着氧化铝是一种离子化合物的化学键形成是由于电子转移。
铝原子的电负性较小,因此,他们捐赠电子氧原子电负性更强。
步骤4:原子氧有6个价电子,需要两个电子来完成他们的八隅体而铝原子有三个电子的价电子层和捐赠他们往往会变得稳定。
步骤5:因此,两个铝原子整体捐赠6个电子三个氧原子。
步骤6:电子转移后,铝原子获得+ 3间(他们捐赠的三个电子),而氧原子获得2间(就像他们已经接受了两个电子)。
步骤7:最后一个路易斯结构的氧化铝是这样的:

氧化铝分子几何
价层电子对斥力(VSEPR)理论,给出了Sidgwick和鲍威尔在1940年,预测分子的形状根据中心原子周围的电子的数量和排列的分子。
这个理论假设一个分子内电子倾向于保持尽可能遥远互相为了避免inter-electronic排斥,因为如果电子保持更紧密的排斥力量增加分子的总能量不稳定。
inter-electronic斥力存在在孤电子以及参与化学键形成一个分子然而,排斥的力量是最强的两个孤对,弱键对。
应当遵循以下步骤来预测分子的结构基于VSEPR理论:
•至少与中心原子电负性很高的原子选择。的氧化铝,铝是最的电负性,因此,选择一个铝原子为中心原子。
•总数为中心原子的价电子数。在氧化铝、铝有三个价电子。
•其他原子的电子参与债券与中心原子的形成也计算在内。
在氧化铝的情况下,所有三个价电子从离子键的三个价电子氧原子。
因此,氧化铝分子中价电子的总数变成了6个。
•价电子层电子对(VSEP)对氧化铝数量= 3(6电子)
•VSEP号码是用来预测分子的几何形状根据下表:
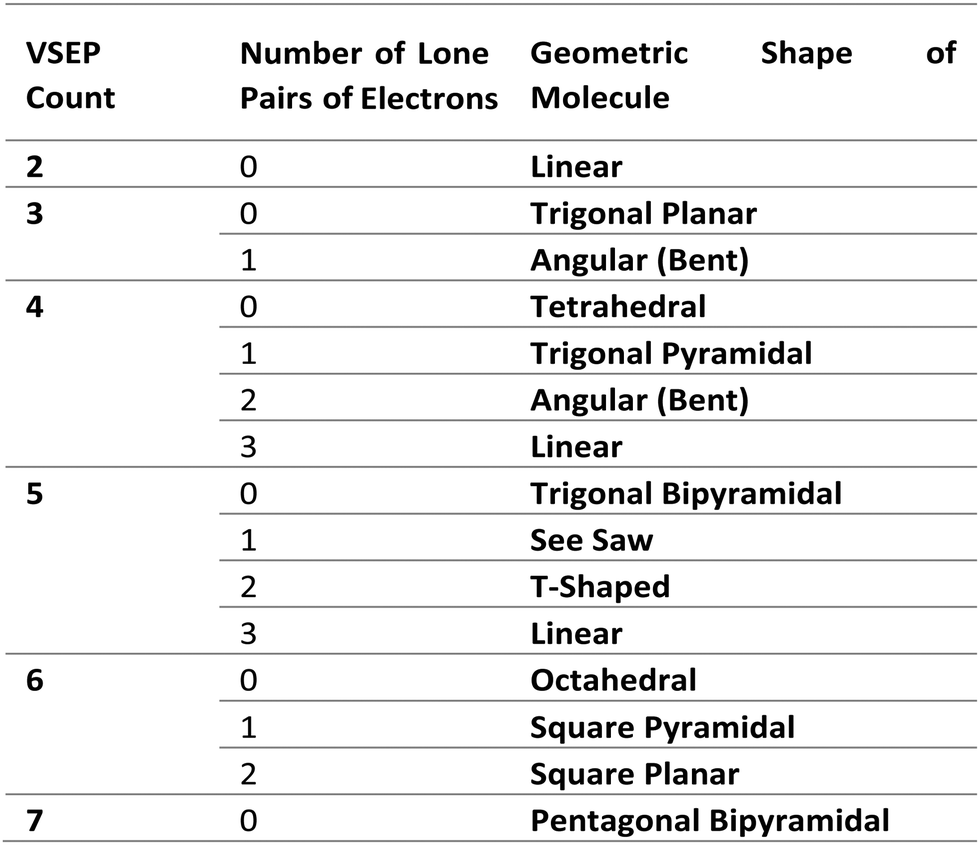
因此,很明显的从上面的表作为氧化铝VSEP数是3,分子应该获得一个三角形的平面形状。
然而,这应当提到,最初氧化铝分子发生在一个三维数组。
因此,一般概念相关的分子几何在这种情况下不适用。

杂交的氧化铝
混合的过程中两个或两个以上的轨道类似的能量称为杂交。
新形成不同于原子轨道杂化轨道参与其形成,形状和能量。
杂交理论于1931年由李纳斯鲍林。
杂化轨道的名字从他们的元素原子轨道viz. dsp3表明一个d,一个年代,和3 p轨道参与这种杂化轨道的形成。
给出的杂交的计算公式为:
杂交=中心原子的西格玛(σ)债券数量+孤对中心原子
确定氧化铝的杂交:
中心原子的σ键数量= 3
中心原子上的孤对数量= 0
因此,杂交= 3 + 0 = 3即sp2杂化
因此,很明显,氧化铝分子sp2杂化。
sp2杂化也被称为三角形杂交。
混合形成的杂化轨道的一个年代和两个p轨道形式三角对称和保持在一个角度120°。
极性的氧化铝

一个条件viz.积极和消极两种截然相反的指控是位于同一分子或原子被称为极性。
在一个分子,极性时由于两个成键原子的电负性的差异。
在氧化铝中,我们已经讨论了它是一个离子分子即它是由电子的转移的铝原子与氧原子。
的氧原子电负性强是由于吸引电子对参与债券本身,因此,开发一个负电荷。
另一方面,铝是阳性赠送其价电子氧气和发展一个正电荷。
因此,氧化铝是一个极性分子离子。
一个这样的分子是ClO3。看看我写的文章的ClO3路易斯结构。
然而,它应该注意,氧化铝是一个三维数组化合物极性和非极性分子的一般原则是不适用的。
属性
氧化铝是一种白色固体也称为刚玉,或刚玉,或铝砂,按其形成或应用程序。
各种氧化铝的性质给出了下面的表格:
| 分子量 | 101.96克/摩尔 |
| 化学公式 | 艾尔2O3 |
| 气味 | 没有气味的 |
| 密度 | 3.987克/厘米3 |
| 熔点 | 2.072°C |
| 沸点 | 2.977°C |
| 在水中溶解度 | 不溶性 |
| 导电性 | 绝缘子 |
| 热导率 | 30 Wm−1K−1 |
| 晶体结构 | 三方晶系的 |
使用
•氧化铝的几个重要的用途是:
•它是用于耐火材料、抛光、陶瓷等。
•氧化铝是一种惰性物质,它是用来填充塑料。
•它是用于化妆品,如防晒霜,脸红,指甲油漆等。
•使用它生产的铝硅酸盐的眼镜。
•在各种工业用作催化剂的反应。
•它是用于制造油漆、身体铠甲,商业纤维材料等。
•它是用作电绝缘体内部电路。
•也用于磨损保护阳极氧化。
结论
•路易斯结构的氧化铝(氧化铝)被表示为:

氧化铝是6•VSEP数量,因此分子应该获得一个三角形的平面形状。
•氧化铝分子sp2杂化。
•氧化铝是一个极性分子离子。
所以,这都是关于氧化铝的路易斯结构。请提出来通过评论你的怀疑。
谢谢! !




